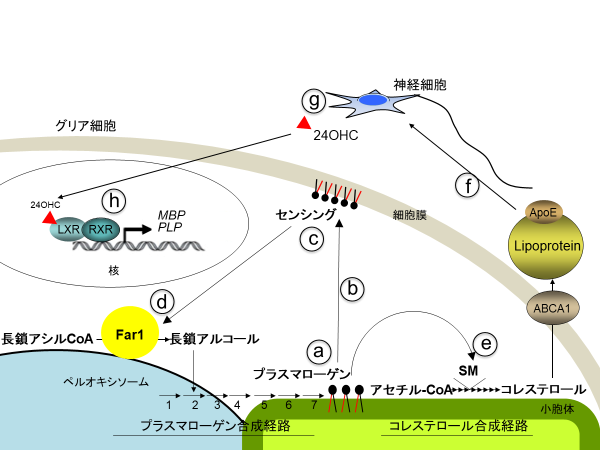
プラズマローゲンの生合成調節とその異常によるコレステロール生合成抑制、ミエリン形成障害のモデル
プラズマローゲンの生合成は、細胞小器官ペルオキシソームで開始され、小胞体で完了する7つのステップを経る(①)。その後、細胞膜へ輸送されたプラズマローゲンは(②)、細胞膜のinner leaflet(内葉)で感知され(③)、プラズマローゲン量の情報はペルオキシソームへと伝達された後、プラズマローゲン合成に必須な長鎖アルコール合成酵素であるfatty acyl-CoA reductase 1 (Far1)の分解を制御する(④)。すなわち、プラズマローゲンの生合成は細胞内プラズマローゲン量を感知するフィードバック機構によるFar1の分解制御で調節される。
プラズマローゲンの生合成障害は(⑤)、コレステロール生合成を担うsqualene monooxygenase (SM)の分解を抑制(⑥)するため、脳においては24,25-エポキシコレステロール(24,25EC)の生合成を増加させるが、コレステロールの合成は抑制される(⑦)。プラズマローゲン合成酵素欠損マウスとプラズマローゲン合成が抑制されるペルオキシソーム形成障害マウスとの小脳で見出したタンパク質の発現変化、コレステロール量の低下、遺伝子発現抑制を赤矢印で記す。グリア細胞で合成されたコレステロールは、リポタンパク質依存的に神経細胞へと輸送され(⑧)、一部のコレステロールは、神経細胞にのみ発現する酵素によって24-hydroxycholesterol (24OHC)へと変換される(⑨)。24OHCは脳に最も多く存在するliver X receptor (LXR)のリガンドである(⑩)。プラズマローゲンの合成障害は、コレステロールおよび24OHCの合成を抑制するため、LXRの標的遺伝子であるミエリン構成タンパク質であるmyelin basic protein (MBP), proteolipid protein 1 (PLP) などの発現が低下し(⑪)、その結果、ミエリン形成が障害されるものと推察される。